Trang muốn chia sẻ với ae về một chủ đề thú vị mà Trang tìm hiểu cũng đã từ khá lâu rồi, nay có thời gian để góp nhặt lên thành một bài viết hoàn chỉnh: Đó là về vi khuẩn, kháng sinh và câu chuyện kháng kháng sinh. Nghe có vẻ hơi khoa học, hơi nhức não một chút nhưng tin Trang, nó bánh cuốn lắm ae.
Từ xưa ơi là xưa, vi khuẩn - mấy "bé hạt tiêu" đơn bào ấy - đã có mặt ở khắp mọi nơi trên Trái Đất rồi. Nào là ao hồ, sông suối, biển cả mênh mông, trên và trong cơ thể những loài to hơn chúng, thậm chí cả những nơi khắc nghiệt nhất, chúng cũng bám trụ được. Mà mỗi loại vi khuẩn lại có một "nhiệm vụ" riêng, có loại thì tốt, có loại thì xấu (tuỳ vào góc nhìn và hướng đánh giá hehe). Ví dụ như, đối với con người, có loại có ích nhờ giúp mình tiêu hoá thức ăn, tạo ra vitamin, dọn dẹp "rác thải" hữu cơ... Nhưng cũng có loại gây bệnh, làm cây cối, động vật, con người bị bệnh, thậm chí là gây ngỏm nữa.Sự hài hòa giữa các loài vi sinh vật đã được duy trì qua hàng tỷ năm tiến hóa.
Thế nhưng, sự cân bằng đó bắt đầu lung lay khi con người phát hiện ra kháng sinh - một thứ vũ khí lợi hại giúp lật ngược ván cờ của mẹ thiên nhiên. Penicillin - loại kháng sinh đầu tiên (được tình cờ phát hiện vào năm 1928 bởi nhà vi sinh học người Scotland Alexander Fleming; sau đó các nhà khoa học Howard Florey, Ernst Boris Chain, và Norman Heatley đã phát triển quy trình sản xuất penicillin ở quy mô công nghiệp vào những năm 1940) đã gây chấn động thế giới vi khuẩn. Chỉ cần một viên có thể càn quét cả “lò” nhà vi khuẩn sau một nốt nhạc :)))
Thế là kỷ nguyên kháng sinh mở ra, kéo theo hàng loạt tiến bộ trong diệt khuẩn, kháng khuẩn và y học. Trong quá trình đó, con người ta lại còn chế ra thêm nhiều loại kháng sinh "xịn sò" khác nữa (như tetracycline, cephalosporin và aminoglycoside), thế là vi khuẩn bị "hội đồng" tơi bời, mang đến nhiều hy vọng mới trong cuộc chiến chống lại bệnh tật. Ở thời kỳ đỉnh cao của kháng sinh, con người có lẽ đã khá tự tin về khả năng “khống chế tự nhiên” và “bất tử” của chính mình.
Nhưng tụi vi khuẩn đâu phải "dạng vừa". Trong cái rủi có cái may, một số con cháu khuẩn "lì lợm" sống sót được, phàm cái gì không ziết được ta sẽ khiến ta mạnh mẽ hơn. Ờ, chúng nó không những không die mà còn nâng cấp, tăng trang bị để "chống trả”. Thế là "Siêu khuẩn" (tức Superbugs) ra đời. Nghe xem có ngầu không :))) Giờ thì con người và vi khuẩn đang "so găng" với nhau trong một cuộc chiến dài hơi, ai cũng muốn dành phần thắng hết: Cuộc chiến của Kháng sinh và Kháng kháng sinh.
Đoạn mở đầu này Trang chỉ "nhá hàng" tới đây thôi. Giờ mới vào sâu nà, Trang sẽ kể tiếp về cách vi khuẩn "lách luật" kháng sinh, rồi con người sẽ làm gì để "chiến đấu" lại nghen.
1. Một tế bào vi khuẩn sẽ gồm những gì?
Kháng sinh là những phân tử đặc hiệu tác động tiêu cực đến các cấu trúc sống của vi khuẩn. Thế nên, để hiểu về kháng sinh, trước hết hãy cùng Trang điểm qua một chút về cấu tạo và các cấu trúc sống của một cụ vi khuẩn hen (gọi là cụ vì liệt tổ liệt tông vi khuẩn đã xuất hiện quá quá lâu trên thế giới này rồi và cả bởi sự thông thái nữa).
Tế bào vi khuẩn, dù có cấu tạo đơn giản hơn nhiều so với tế bào nhân thực (như ở cỏ cây hoa lá, nấm, động vật và con người), vẫn thể hiện khả năng thích nghi cao nhờ các thành phần cấu trúc cơ bản nhưng hiệu quả. Mỗi thành phần trong tế bào vi khuẩn đều đóng vai trò quan trọng, giúp chúng tồn tại và phát triển trong những môi trường khắc nghiệt, từ đó trở thành những sinh vật có vai trò thiết yếu trong hệ sinh thái.
Cấu tạo cơ bản của một tế bào vi khuẩn bao gồm các thành phần chính như màng tế bào, thành tế bào, vùng nhân, ribosome và các cấu trúc phụ trợ khác, tất cả phối hợp để thực hiện các chức năng cần thiết cho sự sống.
a. Vỏ tế bào (bao gồm thành tế bào và màng sinh chất)
- Thành tế bào: Thành tế bào vi khuẩn là một cấu trúc cứng, bao bọc bên ngoài màng sinh chất, cung cấp sự bảo vệ cơ học và duy trì hình dạng cho tế bào. Thành phần chính của thành tế bào là peptidoglycan, một loại polymer bao gồm các chuỗi đường dài liên kết chéo với các đoạn peptide ngắn, tạo nên một cấu trúc khối vững chắc (sự vững chắc này lý giải vì sao đa phần các loại kháng sinh hay cơ chế kháng khuẩn thường tập trung tác động vào việc ngăn tổng hợp thành tế bào mới, chứ ít khi nhắm vào việc phá huỷ thành tế bào sẵn có).
- Ở vi khuẩn Gram dương: Thành tế bào dày, chứa nhiều lớp peptidoglycan và có các teichoic acid giúp tăng cường độ bền vững và khả năng bám dính.
- Ở vi khuẩn Gram âm: Thành tế bào mỏng hơn, chỉ gồm một lớp peptidoglycan mỏng nằm giữa màng sinh chất và màng ngoài. Lớp màng ngoài này chứa lipopolysaccharide (LPS - gọi là nội độc tố), một yếu tố độc lực quan trọng do có khả năng kích hoạt hệ thống miễn dịch một cách mạnh mẽ, tạo thành một hàng rào vật lý để cản trở sự xâm nhập của một số loại kháng sinh vào tế bào vi khuẩn và giúp vi khuẩn bám dính vào các tế bào và mô của vật chủ, né tránh hệ miễn dịch. - Màng sinh chất: Màng sinh chất là một lớp phospholipid kép, đóng vai trò là rào cản chọn lọc, kiểm soát sự trao đổi chất giữa tế bào và môi trường. Màng sinh chất chứa nhiều protein màng tham gia vào quá trình vận chuyển, trao đổi ion và tổng hợp ATP - tạo năng lượng cho sự sống sót của vi khuẩn thông qua hoạt động chuỗi truyền electron, làm xoay “tuabin” ATP synthase có trên màng. Đây cũng là nơi diễn ra nhiều quá trình sinh hóa quan trọng như tổng hợp lipid và chuyển hóa năng lượng.
b. Tế bào chất và các cấu trúc nội bào:
Tế bào chất của vi khuẩn là một môi trường bán lỏng, chứa nhiều nước, ion, các phân tử hữu cơ và protein. Đây là nơi diễn ra hầu hết các hoạt động sinh hóa của tế bào. Trong tế bào chất, các cấu trúc nội bào quan trọng bao gồm:
- Vùng nhân (nucleoid): Không giống tế bào nhân thực, vi khuẩn không có cấu trúc nhân thực sự. DNA của vi khuẩn được tổ chức thành một vùng nhân, thường là một phân tử DNA vòng, siêu xoắn, không được bao bọc bởi màng nhân. Vùng nhân chịu trách nhiệm mang thông tin di truyền và điều khiển các hoạt động sống của tế bào.
- Ribosome: Ribosome vi khuẩn là các bào quan nhỏ, có kích thước 70S, bao gồm hai tiểu đơn vị 50S và 30S (đơn vị S = Svedberg, đơn vị đo lường tốc độ lắng của một hạt trong quá trình ly tâm). Ribosome chiếm khoảng 20% thể tích của một tế bào vi khuẩn. Để cho dễ mường tượng về kích thước của ribosome, ae hãy hình dung thế này nghen: Ribosome 70S thì kích thước đâu đó khoảng 20 nm (nanomet) - tương đương với 1/50000 đường kính của một sợi tóc người thôi ấy, nhỏ mà có võ. Chúng chịu trách nhiệm dịch mã mRNA (phân tử trung gian mang thông tin di truyền từ DNA), đóng vai trò quan trọng trong quá trình tổng hợp protein của vi khuẩn.
- Hạt dự trữ: Trong tế bào chất của vi khuẩn thường chứa các hạt dự trữ, bao gồm glycogen, polyphosphate hoặc lipid, giúp dự trữ năng lượng và nguyên liệu cho các hoạt động trao đổi chất.
c. Các cấu trúc bề mặt
- Lông (flagella): Lông roi là các cấu trúc dài, mảnh, nhô ra khỏi tế bào, giúp vi khuẩn di chuyển trong môi trường. Chúng được cấu tạo từ protein flagellin và chuyển động nhờ sự quay của một cấu trúc gọi là thể gắn động cơ (basal body).
- Pili (lông tơ): Pili là các cấu trúc ngắn hơn flagella, giúp vi khuẩn bám vào bề mặt hoặc tương tác với các tế bào khác. Một loại pili đặc biệt là pili giới tính (sex pili), tham gia vào quá trình trao đổi vật chất di truyền qua tiếp hợp.
- Vỏ nhầy (capsule hoặc slime layer): Một số vi khuẩn có lớp vỏ nhầy bao quanh thành tế bào, được cấu tạo từ polysaccharide hoặc polypeptide. Lớp này giúp vi khuẩn tránh được sự thực bào của hệ miễn dịch và tăng khả năng bám dính vào bề mặt hoặc mô.
d. Các cấu trúc đặc biệt khác:
Một số vi khuẩn có thêm các cấu trúc chuyên biệt để thích nghi với môi trường:
- Nội bào tử (endospore): Là cấu trúc giúp vi khuẩn tồn tại trong điều kiện khắc nghiệt như nhiệt độ cao, môi trường khô cạn hoặc thiếu dinh dưỡng. Nội bào tử có vỏ dày và chứa DNA cùng các enzyme bảo vệ.
- Thylakoid hoặc carboxysome: Có trong các vi khuẩn quang hợp hoặc vi khuẩn cố định carbon để lấy năng lượng, giúp tối ưu hóa quá trình quang hợp hoặc cố định carbon dioxide bằng cách tăng diện tích bề mặt hấp thụ ánh sáng và tạo sự chênh lệch về nồng độ ion H+ ở hai bên màng (H+ chênh lệch thì sẽ gây “chảy” từ nơi cao đến nơi thấp và chảy qua tuabin ATP synthase - như nhà máy thuỷ điện, giúp tạo năng lượng), đồng thời tập trung carbon dioxide và tăng hiệu quả hoạt động của enzyme quang hợp RuBisCO (loại enzyme chuyên dụng để “bắt lấy” CO2 từ môi trường). Sự tối ưu quá trình quang hợp giúp tăng tạo năng lượng và tạo thức ăn ở các loại khuẩn biết quang hợp này.

2. Tổng quan và phân loại các nhóm kháng sinh thường gặp
Trang đã điểm qua về một tế bào vi khuẩn sẽ gồm những gì ở trên rồi, chủ yếu để ae nắm nền tảng nhất định hiểu về các đích tác động của kháng sinh, cho dễ nắm phần sau nè.
Kháng sinh là các hợp chất hóa học được sử dụng để tiêu diệt hoặc ức chế sự phát triển của vi khuẩn, đóng vai trò như một trong những công cụ quan trọng nhất trong y học hiện đại để chống lại các bệnh nhiễm trùng. Chúng hoạt động bằng cách tấn công vào các cấu trúc hoặc quá trình sinh học thiết yếu của vi khuẩn mà không gây hại nhiều đến tế bào của tế bào vật chủ. Điều này đạt được nhờ vào tính đặc hiệu cao của kháng sinh đối với các mục tiêu như thành tế bào, ribosome hoặc enzyme đặc trưng của vi khuẩn.
Cùng với sự phát triển của nền y học trong hàng chục năm, kháng sinh có rất nhiều loại, muôn hình muôn trạng. Kháng sinh có thể được phân loại dựa trên nhiều tiêu chí:
a. Phân loại kháng sinh theo cơ chế tác động
- Kháng sinh ức chế tổng hợp thành tế bào vi khuẩn: Đây là nhóm kháng sinh ngăn cản vi khuẩn tạo ra thành tế bào bền vững, khiến chúng dễ bị phá vỡ và tế bào vi khuẩn không thể phân chia. VD điển hình của nhóm này bao gồm:
- β-lactam (như Penicillin, Cephalosporin - các loại thường gặp): Các kháng sinh này ức chế enzyme transpeptidase, làm gián đoạn liên kết chéo giữa các phân tử peptidoglycan trong thành tế bào. Do đó, vi khuẩn sẽ không thể tổng hợp peptidoglycan mới hoặc duy trì cấu trúc thành tế bào. Hơn nữa, khi môi trường bên ngoài nhiều nước, do thiếu sự neo giữ của thành tế bào, nước đi vào tế bào vi khuẩn sẽ làm tế bào trương phồng và vỡ ra.
- Glycopeptide (như Vancomycin): Chúng ngăn cản sự kéo dài chuỗi peptidoglycan bằng cách thay vì ức chế enzyme transpeptidase, chúng lại trực tiếp “bịt kín” các chuỗi peptide trong peptidoglycan, ngăn cản chúng tạo liên kết chéo (loại liên kết đóng vai trò củng cố cấu trúc thành tế bào nhờ liên kết các chuỗi đường và mở rộng cấu trúc của thành tế bào). Loại kháng sinh này thường được sử dụng trong các trường hợp vi khuẩn Gram dương kháng lại kháng sinh loại β-lactam thường gặp. - Kháng sinh ảnh hưởng đến màng tế bào: Nhóm này phá vỡ tính toàn vẹn của màng tế bào vi khuẩn, dẫn đến rò rỉ ion và các phân tử thiết yếu, khiến vi khuẩn mất khả năng duy trì cân bằng nội môi, ảnh hưởng đến các quá trình trao đổi chất và chức năng tế bào. Cuối cùng, gây chít vi khuẩn.
Lưu ý: Do màng tế bào của tế bào nhân thực (như tế bào người) cũng có cấu trúc lipid, kháng sinh nhóm này có thể gây độc cho tế bào vật chủ, đặc biệt là ở liều cao.
- Polymyxin: Đây là một polypeptide mang điện tích dương, tác động mạnh lên vi khuẩn Gram âm bằng cách liên kết tĩnh điện với lipid A mang điện tích âm của lipopolysaccharide. Sự liên kết này trung hòa điện tích bề mặt của màng ngoài, làm mất ổn định cấu trúc màng. Polymyxin còn chèn vào màng ngoài, làm thay đổi tính thấm của màng. Điều này cho phép các phân tử lớn, ion quan trọng…, vốn khó đi qua, nay có thể tự do xuyên qua màng tế bào, làm rối loạn cân bằng nội môi và chức năng tế bào, gây chít.
- Daptomycin: Khi có mặt canxi, Daptomycin thay đổi cấu trúc và liên kết với màng tế bào vi khuẩn, ưu tiên cho các vùng giàu phosphatidylglycerol. Nhiều phân tử Daptomycin tập hợp lại, tạo thành các oligomer (đơn vị nhỏ liên kết với nhau) trên màng tế bào. Các oligomer daptomycin này chèn sâu vào màng tế bào, tạo thành các lỗ lớn hoặc kênh dẫn ion. Điều này gây mất cân bằng điện hóa, vi khuẩn không thể duy trì sự sống và chít đi. - Kháng sinh ức chế tổng hợp protein: Kháng sinh trong nhóm này nhắm vào ribosome vi khuẩn, ngăn chặn quá trình dịch mã, từ đó ngăn vi khuẩn sản xuất protein. Protein là một trong các nhóm đại phân tử tối quan trọng trong sự sinh tồn của vi khuẩn, đóng nhiều vai trò như cấu trúc, xúc tác, cung cấp năng lượng, dự trữ… → Sự ức chế tạo protein là một đòn đánh “chí tử”.
- Aminoglycoside (như Streptomycin, Gentamicin): Liên kết với tiểu đơn vị 30S của ribosome, gây ức chế hoặc sai sót trong dịch mã tạo protein → Protein không được tạo thành hoặc tạo thành các chuỗi ngắt quãng, không hoàn chỉnh, không có chức năng.
- Macrolide (như Erythromycin, Azithromycin): Gắn vào tiểu đơn vị 50S, ngăn chặn sự kéo dài chuỗi polypeptide → Ngăn cản ribosome “chạy” dọc theo mRNA, protein không được tổng hợp hoàn chỉnh → Ức chế sự phát triển hoặc gây chết tế bào. - Kháng sinh ức chế tổng hợp nucleic acid (các phân tử chuyên dụng cho di truyền): Những kháng sinh này ngăn cản sự nhân đôi hoặc phiên mã DNA, khiến vi khuẩn không thể nhân đôi và sinh sôi. Vi khuẩn không thể nhân đôi, hết vòng đời sẽ tự động bước vào quá trình “tự huỷ”.
- Quinolone (như Ciprofloxacin): Ức chế enzyme DNA gyrase và topoisomerase IV, cần thiết cho sự sao chép DNA.
- Rifamycin (như Rifampin): Ức chế RNA polymerase, cản trở quá trình phiên mã. - Kháng sinh chống chuyển hóa (antimetabolite): Các kháng sinh này ngăn chặn sự tổng hợp các tiền chất cần thiết cho DNA, RNA và protein, từ đó ngăn chặn sự sinh đẻ của vi khuẩn từ trong trứng nước.
- Sulfonamide: Ngăn cản tổng hợp folic acid bằng cách ức chế enzyme dihydropteroate synthase. Folic acid là thành phần cần thiết để sản xuất các đơn phân purine và pyrimidine, thành phần chính trong tổng hợp DNA, RNA và protein của vi khuẩn.
- Trimethoprim: Ức chế enzyme dihydrofolate reductase, cũng là một bước quan trọng trong tổng hợp folic acid.
b. Phân loại kháng sinh theo phổ tác dụng
- Kháng sinh phổ rộng: Chúng tác động lên nhiều loại vi khuẩn, bao gồm cả vi khuẩn Gram dương và Gram âm. VD: Tetracycline, Chloramphenicol, Amoxicillin. Nhóm này hữu ích trong các trường hợp chưa xác định rõ mầm bệnh nên cứ đánh theo hướng thà trém nhầm hơn bỏ sót, nhưng dễ dẫn đến kháng thuốc nếu sử dụng bừa bãi.
- Kháng sinh phổ hẹp: Chúng chỉ nhắm vào một nhóm vi khuẩn cụ thể. VD: Penicillin G (chủ yếu tác động lên vi khuẩn Gram dương), Polymyxin (chỉ tác động lên vi khuẩn Gram âm). Sử dụng nhóm này giúp hạn chế ảnh hưởng đến hệ vi khuẩn có lợi trong cơ thể.
c. Phân loại kháng sinh theo nguồn gốc
- Kháng sinh tự nhiên: Được sản xuất bởi vi sinh vật. VD: Penicillin (nấm Penicillium), Streptomycin (vi khuẩn Streptomyces).
- Kháng sinh bán tổng hợp: Được cải biến từ kháng sinh tự nhiên để tăng hiệu quả hoặc mở rộng phổ tác dụng. VD: Amoxicillin, Ceftriaxone.
- Kháng sinh tổng hợp: Được tổng hợp hoàn toàn trong phòng thí nghiệm, VD: Sulfonamide, Quinolone.
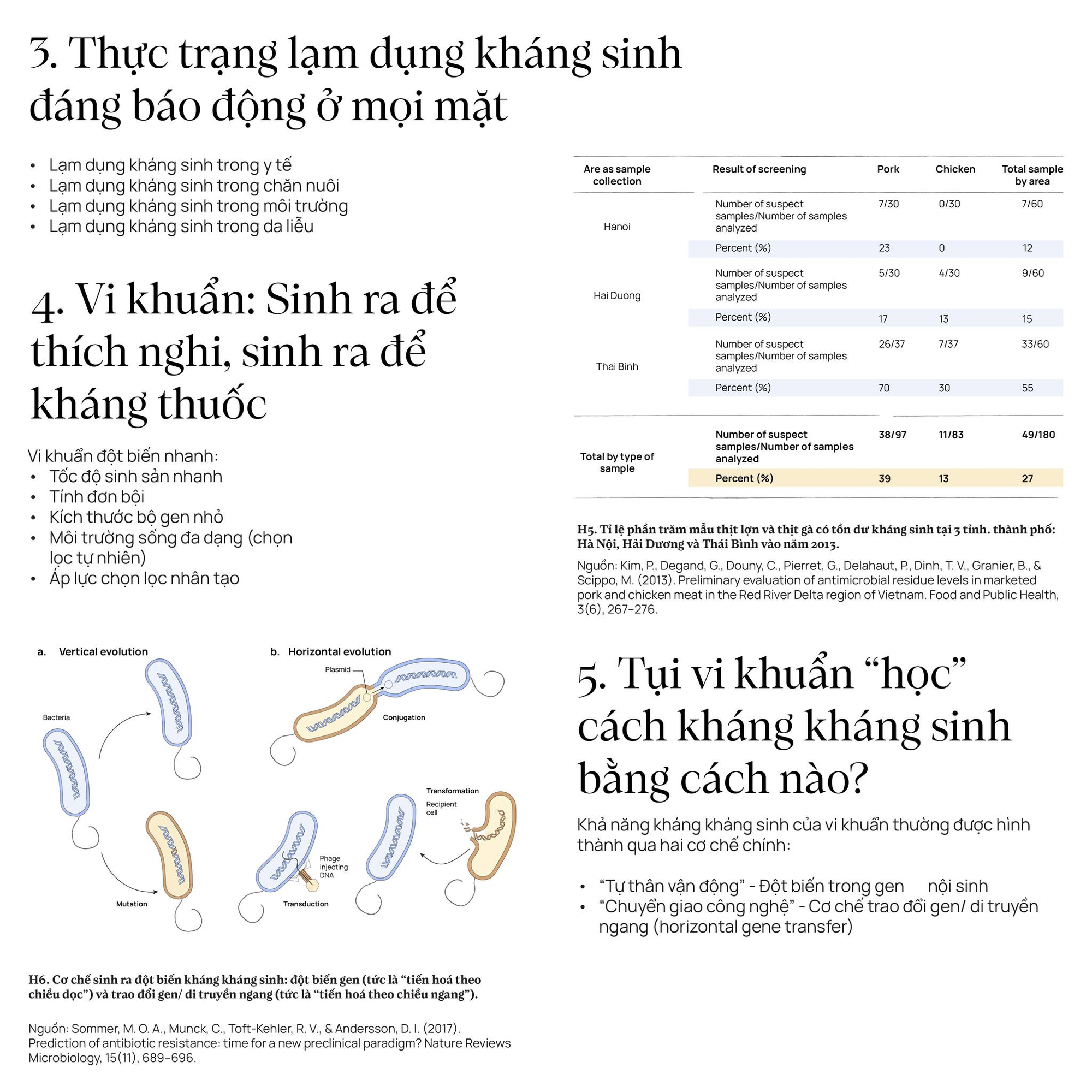
3. Thực trạng lạm dụng kháng sinh đáng báo động ở mọi mặt
Kháng sinh vi diệu là thế, tội gì không dùng? - Chắc hẳn ae đang nghĩ thế phải không.À thì, không phải mỗi ae nghĩ thế đâu… Thực trạng lạm dụng kháng sinh đã và đang là một vấn đề nghiêm trọng trên toàn cầu suốt mấy thập kỷ qua rồi, ảnh hưởng không chỉ đến sức khỏe con người mà còn đến động vật, thực vật và môi trường. Theo báo cáo của Tổ chức Y tế Thế giới (WHO), khoảng 50% kháng sinh trên toàn thế giới được sử dụng không hợp lý, trong đó có việc kê đơn không cần thiết, tự ý sử dụng hoặc sử dụng kháng sinh liều lượng không đúng. Đồng thời, từ năm 2020 đến 2023, Việt Nam ghi nhận gần 270 nghìn ca tử vong liên quan đến kháng kháng sinh, tức gần 70 nghìn ca mỗi năm.Có ae Đồng Điệu nào đã từng ít nhất một lần tự mua tuýp Klenzit-C về chấm mụn chưa nhỉ? Kháng sinh đó. Sao mà Trang thấy việc mua kháng sinh ở Việt Nam dễ quá đi. Dễ đến mức người tiêu dùng quên rằng đấy là “thuốc” luôn ấy.
a. Lạm dụng kháng sinh trong y tế
Trong y tế, việc lạm dụng kháng sinh thường xảy ra dưới nhiều hình thức:
- Kê đơn không hợp lý: Theo WHO, có tới 30 - 60% các trường hợp kê đơn kháng sinh là không cần thiết. VD: Kháng sinh thường được kê cho các bệnh do virus như cảm cúm, viêm họng, trong khi kháng sinh không có tác dụng với virus. Noted: Theo Trang, có thể kháng sinh được kê thêm để phòng ngừa đồng mắc hay bội nhiễm ở những đối tượng nguy cơ (như trẻ em, người lớn tuổi, người có bệnh lý nền, người bị suy giảm miễn dịch). Tuy nhiên, vẫn có những trường hợp dùng kháng sinh là hơi dư thừa (như ở người trẻ, thanh niên sức dài vai rộng chẳng hạn).
- Tự ý sử dụng kháng sinh: Một khảo sát của Tổ chức Hợp tác và Phát triển Kinh tế (OECD) cho thấy ở nhiều quốc gia, từ 30 - 40% người dân tự ý mua kháng sinh mà không có đơn từ bác sĩ. Vẫn có những nhà thuốc sẵn sàng bán thuốc mà không cần đơn. Điều này dẫn đến việc sử dụng kháng sinh sai liều lượng, sai mục đích.
- Thiếu giám sát trong điều trị: Ở các cơ sở y tế thiếu nguồn lực, bệnh nhân thường không được kiểm soát chặt chẽ về việc sử dụng kháng sinh, dẫn đến tình trạng không tuân thủ đúng liệu trình, làm tăng nguy cơ kháng thuốc.
b. Lạm dụng kháng sinh trong chăn nuôi
Ngành chăn nuôi là một nguồn tiêu thụ kháng sinh khổng lồ. Theo báo cáo của Tổ chức Lương thực và Nông nghiệp Liên Hợp Quốc (FAO), hơn 73% lượng kháng sinh toàn cầu được sử dụng trong chăn nuôi để thúc đẩy tăng trưởng và phòng bệnh, thay vì điều trị bệnh. FAO dự báo rằng việc sử dụng kháng sinh ở gia cầm và trang trại heo sẽ tăng hơn 120% ở châu Á vào năm 2030.
Ở một số quốc gia đang phát triển, tỷ lệ này thậm chí còn cao hơn, gây tích tụ kháng sinh trong chuỗi thực phẩm. Một nghiên cứu tại Ấn Độ (2022) do Nukala Ramesh và Hema Tripathi thực hiện phát hiện hơn 76% nông dân chăn nuôi gia cầm dùng kháng sinh một cách vô tội vạ. Một nghiên cứu khác được thực hiện bởi Dang Pham Kim và cộng sự (2013) trên các mẫu thịt lợn được lấy ngẫu nhiên ở ba tỉnh Hà Nội, Hải Dương và Thái Bình cho thấy 39% số mẫu được xác định là có tồn dư kháng sinh.
Việc sử dụng kháng sinh liều thấp trong thức ăn chăn nuôi dẫn đến sự tích lũy vi khuẩn kháng thuốc trong môi trường.Trang giải thích như này cho ae dễ hiểu: Khi kháng sinh được sử dụng liều thấp trong thức ăn chăn nuôi, nó tạo ra một môi trường mà vi khuẩn tiếp xúc với kháng sinh một cách liên tục, nhưng nồng độ không đủ cao để tiêu diệt tất cả vi khuẩn. Trong môi trường này, vi khuẩn nhạy cảm với kháng sinh sẽ bị ức chế hoặc tiêu diệt. Ngược lại, vi khuẩn mang gen kháng thuốc có lợi thế sinh tồn và nhân lên. Quá trình này được gọi là chọn lọc tự nhiên, trong đó kháng sinh đóng vai trò là yếu tố chọn lọc.
Vi khuẩn kháng thuốc có thể tích lũy trong đường ruột của động vật, sau đó lan truyền ra môi trường thông qua phân, nước thải. Vi khuẩn kháng thuốc cũng có thể lây lan sang người thông qua tiếp xúc trực tiếp với động vật, thực phẩm hoặc môi trường.
Một tin đáng chú ý mà Trang nhớ là việc phát hiện vi khuẩn kháng colistin trong lợn ở Trung Quốc giai đoạn 2015 - 2018. Colistin là loại kháng sinh cực mạnh, được xem là "phòng tuyến cuối cùng" của con người trong cuộc chiến chống vi khuẩn kháng thuốc. Sự xuất hiện của vi khuẩn kháng colistin trong lợn có liên quan đến việc lạm dụng kháng sinh này trong chăn nuôi, đặc biệt là việc sử dụng trái phép colistin trong thức ăn chăn nuôi.
c. Lạm dụng kháng sinh trong môi trường
Các chất thải chứa kháng sinh từ bệnh viện, nhà máy dược phẩm và các trang trại chăn nuôi thường không được xử lý đúng cách, gây ô nhiễm nguồn nước và đất. Theo nghiên cứu của Zhang và cộng sự (2015), cùng với nghiên cứu của Ying và cộng sự (2017) tại Trung Quốc cho thấy mỗi năm quốc gia này sử dụng khoảng 162 nghìn tấn kháng sinh, để rồi 58% trong số đó cuối cùng sẽ bị thải ra môi trường đất, nước.
58% của 162 nghìn tấn là một con số rất “khủng”, tương đương với trọng lượng của 236 chiếc máy bay Boeing 747 hay gần 16 nghìn con voi bụi cỏ châu Phi.
Sự thừa mứa kháng sinh trong môi trường tạo điều kiện cho vi khuẩn kháng thuốc “tiến hoá”, hình thành các chủng vi khuẩn đa kháng thuốc, gây ra thách thức lớn cho việc điều trị nhiễm trùng. Cụ thể, những vi khuẩn mang gen kháng thuốc, vốn có thể xuất hiện ngẫu nhiên do đột biến, sẽ có lợi thế sinh tồn vượt trội hơn so với vi khuẩn thông thường.
Qua nhiều thế hệ, tỷ lệ vi khuẩn kháng thuốc trong quần thể tăng lên, lan truyền gen kháng thuốc cho các thế hệ sau và thậm chí cho các vi khuẩn khác thông qua các cơ chế di truyền ngang (Trang sẽ mô tả kỹ hơn cơ chế này ở phần 5).
d. Lạm dụng kháng sinh trong da liễu
Trong lĩnh vực da liễu, lạm dụng kháng sinh là một vấn đề đáng lo ngại và thường không được để tâm bởi đại chúng, đặc biệt trong điều trị các bệnh da liễu mãn tính như mụn trứng cá, viêm da và nhiễm khuẩn da.
Theo Trang, sự thờ ơ này cũng có thể đến một phần từ việc khuẩn kháng kháng sinh ở các bệnh lý da liễu thường ít được báo cáo gây ra hậu quả gì quá nghiêm trọng hay đe doạ đến tính mạng như khuẩn kháng kháng sinh ở các phủ tạng khác. Kháng sinh được sử dụng rộng rãi dưới dạng đường uống, tiêm hoặc bôi tại chỗ, nhưng không phải lúc nào cũng được sử dụng hợp lý.
- Lạm dụng kháng sinh trong điều trị mụn trứng cá:
- Mụn trứng cá là một trong những bệnh da liễu phổ biến nhất, với hơn 9,4% dân số toàn cầu bị ảnh hưởng (theo Global Burden of Disease Study năm 2013). Kháng sinh, đặc biệt là tetracycline, được kê đơn thường xuyên để giảm viêm và ức chế vi khuẩn Cutibacterium acnes.
- Tuy nhiên, một báo cáo của Journal of the American Academy of Dermatology cho thấy hơn 40% bệnh nhân sử dụng kháng sinh kéo dài trên 6 tháng, dẫn đến tình trạng kháng kháng sinh. Nghiên cứu cũng chỉ ra rằng 70 - 90% các dòng vi khuẩn Cutibacterium acnes ở bệnh nhân mụn trứng cá đã kháng với các kháng sinh phổ biến như erythromycin và clindamycin. - Sử dụng kháng sinh không cần thiết trong điều trị nhiễm khuẩn da:
- Trong các bệnh nhiễm khuẩn da như viêm nang lông hoặc viêm mô tế bào, kháng sinh thường được kê đơn một cách tùy tiện, ngay cả khi bệnh có thể tự khỏi hoặc được kiểm soát bằng biện pháp không dùng thuốc kháng sinh.
- Một khảo sát tại Anh năm 2020 cho thấy 25% các trường hợp nhiễm khuẩn da nhẹ vẫn được kê đơn kháng sinh toàn thân thay vì kháng sinh tại chỗ hoặc các liệu pháp thay thế. - Lạm dụng kháng sinh bôi tại chỗ như một loại thuốc không kê đơn:
- Các chế phẩm kháng sinh bôi ngoài da như fusidic acid hoặc mupirocin thường được sử dụng rộng rãi trong điều trị chàm bội nhiễm hoặc các vết thương nhỏ. Tuy nhiên, theo WHO, hơn 50% vi khuẩn Staphylococcus aureus trên da đã kháng với fusidic acid ở một số quốc gia, đặc biệt ở khu vực Đông Nam Á và châu Phi.
- Việc sử dụng kháng sinh bôi tại chỗ không đúng cách (như bôi không đủ liều, không đúng chỉ định) đã tạo ra áp lực chọn lọc lớn, thúc đẩy sự phát triển của vi khuẩn kháng thuốc.
4. Vi khuẩn: Sinh ra để thích nghi, sinh ra để kháng thuốc
Đặc tính dễ đột biến của vi khuẩn là một đặc điểm quan trọng góp phần vào khả năng thích nghi và tiến hóa nhanh chóng của chúng, bao gồm cả khả năng kháng kháng sinh. Có nhiều yếu tố góp phần vào đặc điểm này, có thể kể đến như tốc độ sinh sản nhanh, hệ thống sửa lỗi kém hiệu quả và áp lực chọn lọc từ môi trường (đóng vai trò quan trọng trong việc định hướng sự tiến hóa của vi khuẩn, "lựa chọn" những vi khuẩn có đặc điểm thích nghi tốt).
- Tốc độ sinh sản nhanh: Vi khuẩn có tốc độ sinh sản vượt trội so với các sinh vật đa bào. Chu kỳ phân chia tế bào ngắn, thường chỉ vài phút đến vài giờ, dẫn đến việc sao chép DNA diễn ra liên tục và với tần suất cao. Mỗi lần sao chép, polymerase DNA có thể mắc lỗi, tạo ra các đột biến ngẫu nhiên. Mặc dù vi khuẩn có cơ chế sửa lỗi DNA, nhưng hiệu quả của chúng kém hơn so với sinh vật nhân thực.
Dù nghe có vẻ nghịch lý, hệ thống sửa chữa DNA kém hiệu quả ở vi khuẩn lại góp phần tạo nên khả năng kháng thuốc đáng kể. Vì hệ thống sửa chữa này kém hiệu quả nên vi khuẩn dễ tích lũy các đột biến ngẫu nhiên trong DNA của chúng. Các đột biến này, tuy thường gây hại, đôi khi lại mang đến những thay đổi có lợi, chẳng hạn như biến đổi protein đích của thuốc kháng sinh.
Nói cách khác, cùng với tốc độ sinh sản nhanh, hệ thống sửa chữa DNA kém hiệu quả tạo ra sự đa dạng di truyền cao trong quần thể vi khuẩn, tăng khả năng xuất hiện các biến thể kháng thuốc khi tiếp xúc với kháng sinh. - Tính đơn bội: Hầu hết vi khuẩn là sinh vật đơn bội, nghĩa là chúng chỉ mang một bản sao của mỗi gen. Điều này có nghĩa là bất kỳ đột biến nào xảy ra trên gen đều được biểu hiện ngay lập tức. Ngược lại, sinh vật nhân thực thường là lưỡng bội (diploid), nên một đột biến ở một bản sao gen có thể được "che giấu" bởi bản sao bình thường còn lại (hay được biết đến với tên gọi tương tác trội - lặn hay rộng hơn là tương tác gen). Đặc điểm này làm tăng tốc độ tiến hóa, vì các đột biến có lợi (hoặc có hại) sẽ được thể hiện ngay trong kiểu hình và chịu tác động của chọn lọc tự nhiên gần như ngay lập tức. VD: Đột biến làm tăng khả năng kháng kháng sinh sẽ ngay lập tức giúp vi khuẩn sống sót trong môi trường có kháng sinh.
- Kích thước bộ gen nhỏ: So với sinh vật nhân thực, vi khuẩn có bộ gen nhỏ gọn hơn nhiều. Điều này đồng nghĩa với việc mỗi đột biến có khả năng ảnh hưởng lớn hơn đến kiểu hình của vi khuẩn. Một đột biến nhỏ trên một gen quan trọng có thể gây ra thay đổi đáng kể trong chức năng của tế bào, tạo ra những biến dị mới có thể có lợi hoặc có hại cho vi khuẩn.
- Môi trường sống đa dạng (chọn lọc tự nhiên): Vi khuẩn là những sinh vật có khả năng thích nghi phi thường, tồn tại ở khắp mọi nơi, từ đất, nước, không khí đến cả bên trong cơ thể sinh vật khác. Mỗi môi trường sống đều có những đặc điểm riêng biệt về nhiệt độ, độ pH, nguồn dinh dưỡng và sự hiện diện của các chất hóa học. Chính sự đa dạng này tạo nên vô vàn áp lực chọn lọc khác nhau, thúc đẩy vi khuẩn phải liên tục tiến hóa để tồn tại.
VD: Vi khuẩn sống trong suối nước nóng sẽ phát triển các cơ chế chịu nhiệt, trong khi vi khuẩn sống trong đất nhiễm mặn sẽ tiến hóa để thích nghi với nồng độ muối cao. Sự đa dạng môi trường sống đóng vai trò như một "lò luyện" tạo ra sự phong phú về kiểu gen và kiểu hình ở vi khuẩn. Biết đâu được, dòng đời xô đẩy, gen kháng kháng sinh xuất hiện ngẫu nhiên thì sao ae :))) - Áp lực chọn lọc nhân tạo: Có áp bức thì ắt hẳn sẽ có đấu tranh - câu này đúng ở cả ngữ cảnh về vi khuẩn kháng thuốc. Bên cạnh sự đa dạng môi trường sống, áp lực chọn lọc từ con người cũng đóng vai trò quan trọng trong sự tiến hóa của vi khuẩn, đặc biệt là khả năng kháng kháng sinh.
Kháng sinh gây loại bỏ dần những vi khuẩn nhạy cảm, chỉ những cá thể mang đột biến kháng thuốc mới có thể tồn tại và sinh sôi. Quá trình này thúc đẩy sự lan truyền nhanh chóng của các gen kháng thuốc trong quần thể vi khuẩn.
Ae lưu ý nè: Loại kháng sinh càng mạnh, hàm lượng càng cao, sử dụng càng kéo dài thì áp lực chọn lọc càng lớn, kéo theo sự tăng tỉ lệ thuận của tốc độ chọn lọc tạo chủng khuẩn kháng thuốc. Vậy nên không phải cứ thích thì uống, cứ kháng sinh mạnh mà quất, hay sợ “ngắm gà khoả thân” mà nốc một lần 2 3 viên, uống cả tháng trời đâu ngheng.
5. Tụi vi khuẩn “học” cách kháng kháng sinh bằng cách nào?
Khả năng kháng kháng sinh của vi khuẩn thường được hình thành qua hai cơ chế chính:
- “Tự thân vận động” - Đột biến trong gen nội sinh: Tự đột biến ở gen mã hóa protein đích là một trong những cơ chế quan trọng giúp vi khuẩn tự sinh ra khả năng kháng lại kháng sinh. Bản chất của cơ chế này là sự thay đổi trình tự DNA trong gen mã hóa protein mà kháng sinh thường nhắm đến, dẫn đến sự biến đổi cấu trúc hoặc chức năng của protein đích.
Protein đích của kháng sinh thường là các protein thiết yếu cho sự sống của vi khuẩn, ví dụ như enzyme tham gia tổng hợp thành tế bào, enzyme tham gia sao chép DNA hoặc ribosome - nơi tổng hợp protein. Kháng sinh hoạt động bằng cách liên kết với protein đích và ức chế chức năng của chúng, từ đó ngăn chặn sự phát triển hoặc tiêu diệt vi khuẩn. Tuy nhiên, khi đột biến xảy ra ở gen mã hóa protein đích, nó có thể gây ra những thay đổi sau:
- Giảm ái lực liên kết: Đột biến có thể làm thay đổi cấu trúc không gian của protein đích, khiến kháng sinh khó liên kết hoặc không thể liên kết với protein. VD: Một thay đổi nhỏ trong vị trí liên kết của kháng sinh trên ribosome có thể làm giảm ái lực liên kết của kháng sinh, khiến nó không còn khả năng ức chế quá trình tổng hợp protein.
- Thay đổi cấu trúc protein: Đột biến có thể làm thay đổi cấu trúc tổng thể của protein đích, khiến kháng sinh không còn nhận ra và liên kết được với protein.
- Thay đổi chức năng protein: Trong một số trường hợp, đột biến có thể làm thay đổi chức năng của protein đích, khiến nó vẫn hoạt động bình thường ngay cả khi kháng sinh đã liên kết. VD: Đột biến ở enzyme DNA gyrase khiến enzyme này vẫn có thể tháo xoắn DNA để sao chép, mặc dù đã bị kháng sinh ức chế. - “Chuyển giao công nghệ” - Cơ chế trao đổi gen/ di truyền ngang (horizontal gene transfer): Khác với sinh vật nhân thực, vi khuẩn có khả năng trao đổi vật liệu di truyền trực tiếp và nhanh chóng với nhau thông qua các cơ chế như biến nạp (transformation), tải nạp (transduction) và tiếp hợp (conjugation).
- Biến nạp: Vi khuẩn có thể hấp thụ DNA tự do từ môi trường xung quanh, thường là từ các tế bào vi khuẩn đã chết. Đây là cơ chế chính khiến gen kháng kháng sinh từ loài khuẩn này có thể đột nhiên xuất hiện ở một loài khuẩn khác, chỉ cần chúng có cùng môi trường sống.
- Tải nạp: Virus thực khuẩn thể (bacteriophage) khi nhiễm vào vi khuẩn có thể mang theo một phần DNA của vi khuẩn trước đó và truyền sang vi khuẩn mới.
- Tiếp hợp: Vi khuẩn có thể trao đổi plasmid, những đoạn DNA nhỏ dạng vòng, thông qua tiếp xúc trực tiếp. Tiếp hợp ở vi khuẩn đôi khi được ví như quá trình giao phối ở những sinh vật bậc cao. Tuy nhiên, về bản chất, hai hiện tượng này khác nhau hoàn toàn.
Bên cạnh plasmid, đối tượng “vận chuyển” cho di truyền ngang còn có thể là transposon (“gen nhảy” - có thể tự do bay nhảy từ chỗ này đến chỗ khác trong bộ gen hoặc plasmid) hoặc integron (một cấu trúc di truyền đặc biệt được tìm thấy trong vi khuẩn, có khả năng thu nhận và biểu hiện các gen mới, đặc biệt là các gen kháng kháng sinh - như một "chiếc USB" di truyền, cho phép vi khuẩn dễ dàng "cài đặt" thêm các "phần mềm" mới để thích nghi với môi trường sống).
Các yếu tố và cơ chế này cho phép vi khuẩn thu nhận các gen mới, bao gồm cả những gen mang đột biến, gen kháng kháng sinh từ các cá thể khác trong quần thể hoặc thậm chí từ các loài vi khuẩn khác. Điều này làm tăng tính đa dạng di truyền của quần thể vi khuẩn, tạo điều kiện cho sự xuất hiện của các biến dị mới, tăng tính ổn định của gen kháng trong quần thể và thúc đẩy quá trình tiến hóa tạo “siêu khuẩn”.
6. “Siêu khuẩn” sẽ kháng kháng sinh thông qua những “chiến lược” nào?
Trong bàn cờ sinh tử vô hình giữa con người và vi khuẩn, những kẻ bé nhỏ nhưng mạnh mẽ - các “siêu khuẩn” đã chứng minh rằng chúng là những bậc thầy chiến lược, với khả năng biến hóa không ngừng. Thay vì bị khuất phục, những chiến binh siêu nhỏ này lại triển khai một loạt kế hoạch phòng thủ và phản công tinh vi, từ việc phá hủy kháng sinh, ngụy trang mục tiêu, bơm ngược thuốc ra ngoài, đến việc xây dựng những pháo đài sinh học, siêu khuẩn luôn tìm cách đi trước một bước trong cuộc chiến sinh tồn.
Vậy chúng đã có những tính toán gì để kháng được kháng sinh? Để Trang kể cho ae.

a. Vũ khí phản công đầu tiên: Enzyme tiêu diệt kháng sinh
Trong trận chiến sinh học này, siêu khuẩn luôn mang theo mình những vũ khí hóa học - các enzyme. Hãy tưởng tượng chúng như những thanh kiếm sắc bén được rèn riêng để cắt đứt sức mạnh của kháng sinh. Một VD điển hình là enzyme β-lactamase, loại vũ khí lợi hại có thể phá vỡ vòng β-lactam, cấu trúc cốt lõi của các kháng sinh như penicillin và cephalosporin.
Bên cạnh β-lactamase, một VD nổi bật khác là enzyme carbapenemase, một biến thể mạnh mẽ hơn của β-lactamase, có khả năng phân hủy nhóm kháng sinh carbapenem - vốn được coi là "vũ khí cuối cùng" chống lại vi khuẩn đa kháng thuốc. Klebsiella pneumoniae (một loại khuẩn gram Âm, thường thấy trong ruột hoặc ở những nơi ẩm ướt, có thể gây viêm phổi, viêm màng não và nhiễm trùng máu…) sản xuất carbapenemase (KPC) là một trong những "kẻ thù nguy hiểm" sử dụng enzyme này để vô hiệu hóa các kháng sinh mạnh nhất.
Nhưng không dừng lại ở đó, siêu khuẩn còn sở hữu những "phù thủy biến hình" như các aminoglycoside-modifying enzyme (AMEs), có khả năng biến đổi kháng sinh aminoglycoside bằng cách gắn thêm các nhóm hóa học, khiến kháng sinh trở nên vô dụng. Kết quả? Kháng sinh mất đi sức mạnh, còn vi khuẩn thì tiếp tục ung dung sản xuất protein, nguồn sống thiết yếu của chúng.
b. Chiến thuật ngụy trang: Thay đổi hoặc bảo vệ mục tiêu
Siêu khuẩn biết rằng, để tồn tại, chúng cần bảo vệ những "đích" quan trọng mà kháng sinh nhắm đến. Vì vậy, chúng thay đổi diện mạo hoặc đặt "lá chắn" bảo vệ cho các cấu trúc này. VD: Liên cầu khuẩn MRSA (methicillin-resistant Staphylococcus aureus) đã tinh chỉnh protein liên kết penicillin (PBP2a), khiến kháng sinh β-lactam không thể gắn kết và mất khả năng phá hủy thành tế bào.
Còn với tetracycline, một kháng sinh mạnh mẽ nhắm vào ribosome, siêu khuẩn lại triệu tập "người bảo vệ" TetM để ngăn không cho kháng sinh tiếp cận ribosome. Với cách này, siêu khuẩn biến mình thành những mục tiêu bất khả xâm phạm.
Một VD khác là vi khuẩn Mycobacterium tuberculosis - tác nhân gây bệnh lao. Chúng đột biến gen rpoB (mã hóa enzyme RNA polymerase) để kháng lại rifampin, một trong những kháng sinh hàng đầu trong điều trị lao. Nhờ sự thay đổi này, rifampin không thể gắn vào RNA polymerase để ngăn cản quá trình tổng hợp RNA (chính là nền tảng của quá trình phiên mã), khiến vi khuẩn tiếp tục phát triển mạnh mẽ.
c. Con đường thoát hiểm: Hệ thống bơm ngược
Siêu khuẩn còn có khả năng phát triển những chiếc "máy bơm mini" - các efflux pumps, giúp đẩy kháng sinh ra ngoài trước khi chúng đạt được nồng độ tiêu diệt. Hãy tưởng tượng các máy bơm này như những cánh cửa thoát hiểm khẩn cấp, được điều khiển bởi hệ thống phức tạp như AcrAB-TolC ở vi khuẩn Escherichia coli. Những "cánh cửa" này không chỉ hoạt động với một loại thuốc mà còn chống lại nhiều nhóm kháng sinh như tetracycline, fluoroquinolone và macrolide, tạo nên khả năng kháng đa thuốc đáng sợ.
Một VD khác minh họa cho cơ chế bơm ngược là hệ thống NorA efflux pump ở vi khuẩn Staphylococcus aureus. Hệ thống này đặc biệt hiệu quả trong việc bơm các kháng sinh fluoroquinolone ra ngoài, khiến thuốc không thể đạt được nồng độ cần thiết để tiêu diệt vi khuẩn.
Hơn nữa, Pseudomonas aeruginosa với hệ thống MexAB-OprM cũng được biết đến là "chuyên gia bơm ngược", giúp chúng kháng lại không chỉ fluoroquinolone mà còn các kháng sinh nhóm aminoglycoside và β-lactam.
d. Lớp giáp bảo vệ: Giảm tính thấm của màng tế bào
Khi đối mặt với mối đe dọa, siêu khuẩn không ngần ngại củng cố "thành trì" của mình bằng cách làm giảm tính thấm của màng tế bào. Hãy nghĩ đến những bức tường kiên cố, nơi mà các kênh protein (porin) bị thu hẹp hoặc biến mất, ngăn không cho kháng sinh xuyên qua. Chiến thuật này thường thấy ở những kẻ thù nguy hiểm như Pseudomonas aeruginosa, một bậc thầy phòng thủ đối với kháng sinh carbapenem.
Vi khuẩn Escherichia coli kháng colistin (loại kháng sinh mà nãy Trang nhắc đến ở đoạn về lạm dụng kháng sinh trong chăn nuôi ở Trung Quốc đó) cũng là một VD đáng chú ý. Chúng sửa đổi cấu trúc lipid A trên màng ngoài bằng cách thêm nhóm phosphoethanolamine, làm giảm ái lực của kháng sinh colistin với màng tế bào. Điều này giúp chúng né tránh tác động của loại kháng sinh thường được sử dụng như lựa chọn cuối cùng trong điều trị nhiễm khuẩn Gram âm đa kháng thuốc.
e. Kế hoạch dự phòng: Con đường chuyển hóa thay thế
Siêu khuẩn cũng giống như những nhà khoa học tài ba, luôn tìm ra giải pháp sáng tạo để duy trì sự sống. Khi đối mặt với sulfonamide - loại kháng sinh nhắm vào enzyme dihydropteroate synthase (DHPS) trong tổng hợp folate (tiền tố tổng hợp nên vật chất di truyền của vi khuẩn), chúng ngay lập tức "nâng cấp" enzyme này hoặc sử dụng folate từ môi trường ngoài. Đây chẳng khác nào một cuộc cách mạng công nghiệp vi mô, giúp vi khuẩn tiếp tục sống sót bất chấp mọi trở ngại.
Vi khuẩn Enterococcus faecalis kháng vancomycin cũng là một VD điển hình. Chúng thay thế D-alanine-D-alanine trong thành phần peptidoglycan của thành tế bào bằng D-alanine-D-lactate, làm giảm ái lực của kháng sinh vancomycin với thành tế bào, từ đó duy trì khả năng sinh trưởng dù có mặt kháng sinh.
f. Sản xuất dư thừa: Tăng lượng đích tác động
Một cách khôn ngoan khác của siêu khuẩn là sản xuất số lượng lớn enzyme hoặc protein mà kháng sinh nhắm tới, khiến thuốc như bị "loãng" tác dụng. Trong cuộc đấu trí này, vi khuẩn chẳng khác nào những nhà sản xuất hàng loạt, tăng cường lượng enzyme dihydrofolate reductase (DHFR - một enzyme quan trọng trong con đường tổng hợp folic acid của vi khuẩn) để đối phó với kháng sinh trimethoprim.
Vi khuẩn Staphylococcus aureus kháng Linezolid cũng sử dụng chiến thuật này bằng cách tăng cường sản xuất ribosome. Điều này khiến Linezolid, một loại kháng sinh nhằm vào tiểu đơn vị 50S của ribosome, không còn đủ mạnh để ngăn cản quá trình tổng hợp protein, giúp vi khuẩn duy trì sự sống.
g. Hậu phương vững chắc: Màng sinh học
Màng sinh học (biofilm) là nơi siêu khuẩn xây dựng một xã hội thu nhỏ, nơi chúng cộng sinh, hỗ trợ nhau để tồn tại. Bên trong lớp "pháo đài" polysaccharide này, vi khuẩn phân công nhiệm vụ rõ ràng: một số bảo vệ, một số sản xuất tài nguyên và một số khác - các "tế bào ngủ đông" - sẵn sàng hồi sinh khi môi trường thuận lợi. Chính khả năng này khiến kháng sinh khó tiếp cận và tiêu diệt toàn bộ vi khuẩn trong màng sinh học.
h. Tăng cường sửa chữa DNA: Hệ thống hồi phục
Fluoroquinolone, một loại kháng sinh mạnh mẽ, tấn công DNA vi khuẩn bằng cách ức chế enzyme gyrase - là một loại enzyme thuộc họ topoisomerase, đóng vai trò quan trọng trong quá trình sao chép và duy trì cấu trúc DNA thông qua việc giảm căng xoắn DNA, tạo thuận lợi cho sự sao chép và phiên mã; hoặc tạo siêu xoắn âm (negative supercoiling) giúp tối ưu kích thước DNA để thực hiện phân chia.
Nhưng siêu khuẩn không dễ dàng chịu thua. Chúng kích hoạt hệ thống SOS để sửa chữa tổn thương DNA, như thể tự chữa lành vết thương sau mỗi đợt tấn công.
Một VD khác về khả năng sửa chữa DNA là Helicobacter pylori, vi khuẩn gây loét dạ dày. Chúng sử dụng enzyme RecA và hệ thống SOS để sửa chữa tổn thương DNA do kháng sinh metronidazole gây ra. Nhờ cơ chế này, H. pylori có thể khôi phục DNA và kháng lại những nỗ lực tiêu diệt từ kháng sinh.
Thật ra sách vở một vài nơi còn liệt kê thêm một cơ chế nữa, đó là sự thu nhận gen kháng thuốc thông qua hiện tượng di truyền ngang. Nhưng đối với Trang, Trang sẽ xếp nó vào cơ chế vi khuẩn “học” cách kháng thuốc (tức là thu nhận kỹ năng kháng thuốc) hơn là một cơ chế kháng thuốc đúng nghĩa (là tác động trực tiếp hay gián tiếp đến sự hoạt động của kháng sinh). Trang có mô tả chi tiết về di truyền ngang ở mục 5, ae cần hay lỡ quên thì lướt lên đọc lại nghen.
Nói về mấy cách thức kháng kháng sinh của “siêu khuẩn” này, Trang thấy cái nào cũng đáng gờm và có cái hay hết ấy. Y như cờ tướng, hai bên cứ phải "đấu trí" với nhau từng nước đi. Quy đi quy lại thì cũng chỉ loanh quanh việc tính toán, ra nước đi của mình và suy nghĩ để chặn hay phá nước đi của đối thủ mà thôi. Lời “ví von văn vở” của một thanh niên đang luyện chơi cờ tướng
Để mà bình ra một cơ chế mà Trang cảm thấy ấn tượng nhất trong cả thảy các cơ chế trên, có lẽ Trang sẽ chọn cơ chế g. Hậu phương vững chắc: Màng sinh học.
“Bà Trang này kì khôi ghê, sao bao cơ chế hay không chọn?” - Ae bình tĩnh đê, nghe Trang đưa ra lý do nè. Tại sao đoạn về cơ chế đó lại ngắn như vậy? Vì đây là cơ chế ít được để tâm nhất.
Nhưng Trang lại thấy nó vừa khá hay ho, vừa có gì đó bí ẩn và cần được khai phá. Điểm nổi bật của cơ chế này chính là, thay vì như các cơ chế khác, tức là thường là cơ chế kháng thuốc trên từng con khuẩn một, sự kháng kháng sinh của màng sinh học là một kiểu “kỹ năng tập thể”.
Nói về cái màng sinh học của vi khuẩn á, trước đây ít ai để ý đến vai trò của nó trong mấy bệnh ngoài da lắm. Nhưng mà giờ thì khác rồi, người ta phát hiện ra là nó đóng vai trò quan trọng trong nhiều bệnh ngoài da dai dẳng, từ viêm nang lông, chàm bội nhiễm cho đến mấy cái vết thương khó lành ở người bị tiểu đường hay bỏng. Cái màng sinh học này không chỉ đơn thuần là chỗ trú ẩn của vi khuẩn đâu nha, mà nó còn như một cái "pháo đài" giúp tụi nó kháng thuốc cực kỳ hiệu quả nữa.
Cái "khoai" ở đây là, cơ chế kháng kháng sinh của màng sinh học rất khó nhận biết. Bởi vì nó là kiểu "chung sức chung lòng" của cả tập thể vi khuẩn, chứ không phải do đặc điểm riêng của từng con vi khuẩn. Thành ra xét nghiệm thông thường, nuôi cấy khuẩn lạc, cấy chuyền, cấy đĩa các kiểu khó mà phát hiện ra được. Nhiều khi, mình tách từng con vi khuẩn ra thì thấy nó có kháng thuốc gì mấy đâu.
Vậy mà khi tụi nó "hợp sức" lại trong cái màng sinh học thì thuốc men lại "bó tay". Trước đây, người ta cứ tưởng tụi nó chỉ vô tình "dính" vào lớp màng nhầy thôi, ai dè đâu tụi nó "khôn" hơn chúng mình tưởng tượng nhiều.
Các vết thương có màng sinh học này rất khó lành, cứ bị phủ một lớp màng nhầy hay váng nhớt nhớt. Đó chính là "sản phẩm" của tụi vi khuẩn, giúp chúng "né" thuốc với cả hệ miễn dịch của mình.Nói chung, tụi vi khuẩn trong màng sinh học này nó "khôn" lắm. Chúng biết "hợp tác", "phân công lao động" rõ ràng, con nào con nấy có nhiệm vụ cụ thể. Con thì lo bảo vệ, con thì lo kiếm "lương thực", con thì sẵn sàng "xâm chiếm" vùng đất mới. Nhờ vậy mà cái màng sinh học nó mới "bất khả xâm phạm" như vậy.
Đấy, ae thấy cái màng sinh học này hay không nào?
7. Nhân loại có gì trong tay trước cuộc giáp lá cà với “siêu khuẩn”
Trong cuộc chiến này, không phải con người hoàn toàn bất lực. Với các nguồn lực sẵn có từ y học hiện đại, công nghệ sinh học và các chính sách quản lý, chúng ta vẫn có những công cụ mạnh mẽ để chống lại “siêu khuẩn”.
a. Các kháng sinh sẵn có và tối ưu hóa việc sử dụng
Mặc dù nhiều loại kháng sinh đã mất đi hiệu quả do sự kháng thuốc, nhân loại vẫn còn trong tay một số kháng sinh mạnh mẽ, đặc biệt là những "vũ khí cuối cùng" như carbapenem, vancomycin, colistin. Những thuốc này được sử dụng cẩn trọng trong các trường hợp nhiễm trùng nghiêm trọng bởi vi khuẩn đa kháng thuốc.
Tuy nhiên, việc chỉ đơn thuần dựa vào các kháng sinh hiện có không đủ để đối phó với tốc độ tiến hóa của vi khuẩn. Do đó, tối ưu hóa sử dụng kháng sinh là điều cốt yếu. Theo Tổ chức Y tế Thế giới (WHO), việc triển khai phác đồ điều trị hợp lý, kết hợp xét nghiệm vi sinh nhanh để xác định chính xác tác nhân gây bệnh, có thể giảm đáng kể việc kê toa không cần thiết, kéo dài tuổi thọ của các kháng sinh hiện hành.
Ở các bệnh viện tiên tiến, việc sử dụng công nghệ PCR (Polymerase Chain Reaction - công nghệ xét nghiệm này có lẽ các Đồng Điệu đã nghe đến nhiều trong đợt dịch COVID-19 nè) để phát hiện nhanh vi khuẩn kháng kháng sinh, giúp giảm tỷ lệ kê kháng sinh phổ rộng không cần thiết đến 20 - 30%.
b. Sự phát triển của các kháng sinh mới
Dù việc phát triển kháng sinh mới đang gặp nhiều trở ngại - như chi phí cao và sự hạn chế trong nghiên cứu lâm sàng - nhân loại vẫn đạt được những tiến bộ đáng kể. Các kháng sinh mới, như ceftazidime-avibactam (một β-lactam kết hợp chất ức chế β-lactamase), đã được phát triển để đối phó với các vi khuẩn kháng carbapenem.
Hơn nữa, sự phát triển của các kháng sinh tổng hợp và bán tổng hợp đang mở ra những cơ hội mới. Các nhà nghiên cứu tập trung vào việc cải tiến các nhóm thuốc cổ điển như aminoglycoside hoặc tetracycline để tăng hiệu quả và giảm nguy cơ kháng thuốc.
c. Công nghệ sinh học - Tương lai của cuộc chiến
Công nghệ sinh học đã trở thành một trong những đồng minh lớn nhất của con người trong cuộc chiến với siêu khuẩn. Các công nghệ tiên tiến bao gồm:
- Liệu pháp bacteriophage: Bacteriophage - virus tấn công vi khuẩn - đang được nghiên cứu như một phương pháp điều trị thay thế hoặc bổ sung cho kháng sinh. Bacteriophage có khả năng nhắm mục tiêu chính xác vào vi khuẩn mà không ảnh hưởng đến các vi khuẩn có lợi hoặc tế bào người. Một nghiên cứu tại Đại học Yale (2021) đã chứng minh rằng liệu pháp này hiệu quả trong việc tiêu diệt Pseudomonas aeruginosa kháng thuốc.
- Công nghệ CRISPR-Cas9: Hệ thống CRISPR-Cas9 được sử dụng để chỉnh sửa gen của vi khuẩn, loại bỏ gen kháng kháng sinh hoặc tiêu diệt vi khuẩn mục tiêu. Đây là một phương pháp hứa hẹn để xử lý vi khuẩn đa kháng thuốc mà không gây hại đến các vi sinh vật có lợi.
- Kháng sinh peptide: Peptide kháng khuẩn (AMPs) là những phân tử nhỏ có khả năng phá hủy màng tế bào vi khuẩn. Chúng có khả năng tiêu diệt vi khuẩn mà không gây kháng thuốc do không nhắm đến các đích cụ thể.
d. Ứng dụng các hoạt chất giảm khuẩn phi kháng sinh
Hoạt chất diệt khuẩn phi kháng sinh là các hợp chất hóa học hoặc tự nhiên có khả năng tiêu diệt hoặc ức chế sự phát triển của vi sinh vật (bao gồm vi khuẩn, nấm, virus) mà không thuộc nhóm kháng sinh truyền thống.
Chúng hoạt động dựa trên các cơ chế khác biệt hơn so với các kháng sinh (tức là đánh vào những điểm chung hơn, chung đến mức vi sinh vật không thể “nâng trang bị” để chống lại nó được - VD: cồn khô gây biến tính protein, mà một tế bào sinh ra muốn kháng cồn thì phải không có protein, chính là một điều bất khả thi trên phương diện sinh học tế bào), giúp giảm nguy cơ tạo ra kháng thuốc - một trong những thách thức lớn nhất của y học hiện đại.
#Noted: Nhấn mạnh với ae là không có thành phần xấu chỉ là dễ rủi ro nếu chúng ta không điêu luyện.
- Iodine, từ lâu đã được sử dụng trong sát trùng vết thương, hoạt động bằng cách oxy hóa protein và DNA của vi khuẩn, khiến chúng bị tiêu diệt nhanh chóng. Các dạng thức bào chế của iodine đang ngày càng đa dạng, tiêu biểu như dạng nước súc miệng để giảm viêm họng.
- Cồn khô, phổ biến dưới dạng ethanol hoặc isopropanol, làm biến tính protein và phá hủy màng lipid của vi khuẩn, phù hợp trong khử khuẩn da và dụng cụ y tế. Trong mỹ phẩm, nồng độ cồn khô ở mỗi sản phẩm nên được R&D kỹ càng để tối ưu được hiệu quả giảm khuẩn và tối thiểu hậu quả gây khô.
Một nghiên cứu vào năm 2023 của Shijie Jian và cộng sự cho thấy khả năng giảm sinh độc tố và giảm kháng kháng sinh ngay cả khi sử dụng ethanol liều thấp liên tục (~0.1%) trên dòng khuẩn Pseudomonas aeruginosa kháng thuốc. - Chlorhexidine, với cơ chế là một ion gốc hữu cơ mang 1 gốc clo (Cl) mang điện tích dương, có đặc tính liên kết mạnh và không đặc hiệu vào màng tế bào để gây “lủng” màng, thường gặp trong các sản phẩm chăm sóc răng miệng không kê đơn.
- Oxy già (hydrogen peroxide) và Benzoyl Peroxide (BPO) là 2 hoạt chất mang tính oxy hoá mạnh, gây stress oxy hoá cho vi khuẩn nhờ tạo một lượng lớn gốc tự do tại chỗ. Ngoài tác dụng oxy hóa, oxy già ở dạng lỏng còn có tác dụng cơ học. Khi tiếp xúc với vết thương, oxy già tạo ra bọt khí oxy. Các bọt khí này giúp loại bỏ các mảnh vụn mô chết, mủ và vi khuẩn ra khỏi vết thương, tạo điều kiện cho quá trình lành vết thương diễn ra thuận lợi.
Trang kể ae nghe, dạo gần đây Trang đã mày mò đưa hai hoạt chất diệt khuẩn phi kháng sinh khá hay ho vô sản phẩm trong quá trình R&D rồi, đó là nano bạc (hay còn gọi là colloidal silver) với terpinen-4-ol (một thành phần chính trong tinh dầu tràm trà) á. Trang đã tìm hiểu được những gì? Ae đọc qua với Trang hen.
- Nano bạc (colloidal silver), với kích thước siêu nhỏ, có khả năng gắn kết vào màng tế bào và phá vỡ cấu trúc vi khuẩn, được ứng dụng trong y tế và công nghiệp mỹ phẩm. Một số nghiên cứu hay ho mà Trang tìm được về thành phần này có thể kể đến là:
- Về Hoạt tính kháng khuẩn và ngăn chặn hình thành màng sinh học của vi khuẩn gây mụn (2024): Nano bạc với kích thước siêu nhỏ (~22nm) có diện tích bề mặt rất lớn so với thể tích của chúng, điều này đóng vai trò quan trọng trong khả năng kháng khuẩn. Diện tích bề mặt lớn giúp các hạt nano bạc tiếp xúc nhiều hơn với màng tế bào vi khuẩn, làm tăng hiệu quả tương tác trực tiếp.
Tương tác này có thể phá vỡ màng tế bào vi khuẩn, dẫn đến rò rỉ các thành phần bên trong tế bào và làm suy yếu cấu trúc của vi khuẩn. Hơn nữa, diện tích bề mặt lớn cũng cho phép nano bạc giải phóng ion bạc (Ag+) một cách hiệu quả hơn, các ion này tiếp tục xâm nhập vào tế bào vi khuẩn, gây rối loạn các quá trình trao đổi chất và dẫn đến sự bất hoạt của vi khuẩn.
Đặc biệt, nano bạc còn có hiệu quả vượt trội trong việc ức chế sự hình thành màng sinh học, làm giảm đáng kể hoạt động trao đổi chất của màng đã hình thành, đồng thời tiêu diệt vi khuẩn bám trên màng. Nano bạc cho thấy hiệu quả nổi bật ngay cả ở nồng độ thấp, khẳng định tiềm năng lớn trong điều trị vi khuẩn kháng kháng sinh. Trong số các thành phần trị mụn kỳ cựu hiện nay, “Old but Gold”, thực sự Trang đánh giá cao Nano bạc.
- Về Hoạt tính kháng các chủng vi khuẩn kháng kháng sinh (2020): Các thử nghiệm cho thấy nano bạc có hiệu quả tiêu diệt vi khuẩn ở nồng độ từ 4 - 8 mg/L đối với 90% chủng vi khuẩn, bao gồm cả các vi khuẩn kháng đa kháng sinh như Acinetobacter baumannii, Escherichia coli và Staphylococcus aureus. Các vi khuẩn Gram dương, điển hình như S. aureus, có xu hướng kháng bạc hơn do cấu trúc thành tế bào dày chứa nhiều peptidoglycan. Tuy nhiên, ngay cả những vi khuẩn này cũng bị tiêu diệt khi nồng độ nano bạc được tăng dần, chứng tỏ hiệu quả vượt trội của nó trong việc đối phó với vi khuẩn kháng thuốc.
- Về Hoạt tính kháng nấm Malassezia (2019): Nghiên cứu đã đánh giá khả năng kháng nấm của các hạt nano bạc đối với Malassezia furfur, một loại nấm gây bệnh ngoài da phổ biến. Nano bạc tương tác với thành tế bào nấm thông qua cơ chế bám dính không đặc hiệu, làm tổn thương cấu trúc tế bào, tạo ra các gốc oxy hóa mạnh (ROS) và thay đổi tính thấm màng, dẫn đến rò rỉ ion và gián đoạn hoạt động của các enzyme chuỗi hô hấp. Những tác động này gây ức chế quá trình sao chép DNA, bất hoạt protein và cuối cùng là tiêu diệt tế bào nấm.
Ngoài ra, nano bạc có khả năng giải phóng ion bạc một cách bền vững, duy trì hiệu quả kháng nấm lâu dài. Khi kết hợp với ketoconazole, một thuốc kháng nấm truyền thống, nano bạc không chỉ tương thích mà còn tạo ra hiệu quả hiệp đồng, tăng cường khả năng điều trị. - Đặc biệt, terpinen-4-ol, một thành phần chính trong tinh dầu tràm trà, có khả năng phá vỡ màng tế bào vi khuẩn và chống viêm, đang được sử dụng trong điều trị mụn và nhiễm trùng nhẹ. Một số nghiên cứu mà Trang đã tổng hợp được bao gồm:
- Khả năng kháng liên cầu khuẩn Streptococcus agalactiae (2018): Terpinen-4-ol cho thấy hoạt tính diệt khuẩn mạnh với MIC (nồng độ ức chế tối thiểu) là 98 µg/mL và MBC (nồng độ diệt khuẩn tối thiểu) là 196 µg/mL. Hợp chất này gây tổn thương có chọn lọc đến màng và thành tế bào vi khuẩn, dẫn đến hiện tượng plasmolysis (thoát nước bào tương) và làm mất cấu trúc tế bào vi khuẩn. Đồng thời, terpinen-4-ol còn cản trở tổng hợp protein và ức chế quá trình sao chép cũng như sửa chữa DNA của vi sinh vật.
- Khả năng kháng khuẩn và kháng nấm phổ rộng (2001): Terpinen-4-ol thể hiện hoạt tính kháng khuẩn và kháng nấm mạnh đối với nhiều loại vi khuẩn và nấm, bao gồm cả các dòng kháng kháng sinh như MRSA. MIC của terpinen-4-ol dao động từ 0.5% đến 8%, tùy thuộc vào từng chủng vi khuẩn hoặc nấm. Candida spp. và Staphylococcus aureus là những vi sinh vật nhạy cảm nhất, với MIC từ 0.5% đến 1%, trong khi các chủng như Pseudomonas aeruginosa và liên cầu khuẩn có MIC >8%, cho thấy khả năng kháng lại cao hơn.
- Khả năng đảo ngược kháng kháng sinh (tức là khôi phục lại hiệu quả của kháng sinh đối với vi khuẩn kháng thuốc) và ức chế tạo màng sinh học (2020): Terpinen-4-ol cho thấy hiệu quả ấn tượng trong việc đảo ngược sự kháng kháng sinh và ngăn chặn sự hình thành màng sinh học của Staphylococcus aureus. Hợp chất này liên kết với protein gắn penicillin (PBP2a), một enzyme quan trọng trong việc tổng hợp thành tế bào của vi khuẩn MRSA, làm enzyme này nhạy cảm trở lại với kháng sinh. Ngoài ra, terpinen-4-ol còn ức chế >90% sự hình thành màng sinh học ở nồng độ từ 2MIC đến 4MIC. Ngay cả ở nồng độ dưới MIC, hiệu quả ức chế vẫn đạt ~80%.
e. Vaccine - Vũ khí phòng ngừa hiệu quả
Vaccine được xem là giải pháp dài hạn để ngăn chặn nhiễm trùng do vi khuẩn, giảm nhu cầu sử dụng kháng sinh. Các vaccine như vaccine phòng phế cầu khuẩn (Streptococcus pneumoniae) hoặc vaccine phòng Haemophilus influenzae đã giúp giảm đáng kể các trường hợp nhiễm trùng đường hô hấp phải điều trị bằng kháng sinh.
Hiện tại, nhiều vaccine mới đang được phát triển để đối phó với các vi khuẩn nguy hiểm như Staphylococcus aureus hoặc Klebsiella pneumoniae. Nếu thành công, chúng sẽ đóng vai trò quan trọng trong việc giảm áp lực kháng sinh lên vi khuẩn.Nhưng vaccine cũng có lắm chuyện phải lo, đừng tiêm bừa bãi, cân nhắc và tìm hiểu trước khi quyết định tiêm nha ae.
f. Chính sách và kiểm soát toàn cầu
Cuối cùng, cuộc chiến với siêu khuẩn không chỉ phụ thuộc vào các giải pháp khoa học mà còn đòi hỏi sự hợp tác toàn cầu. Các chương trình như Kế hoạch Hành động Toàn cầu về Kháng Kháng Sinh (GAP-AMR) của WHO đã tập trung vào các biện pháp kiểm soát như:
- Giám sát việc sử dụng kháng sinh trong y tế và nông nghiệp.
- Ban hành quy định cấm sử dụng kháng sinh như chất kích thích tăng trưởng trong chăn nuôi.
- Đẩy mạnh giáo dục cộng đồng về tác hại của việc lạm dụng kháng sinh.
Một VD thành công là Đan Mạch. Năm 1995, Đan Mạch đã thiết lập Chương trình Giám sát và Nghiên cứu Kháng kháng sinh Tích hợp Quốc gia (DANMAP) để theo dõi việc sử dụng kháng sinh trong chăn nuôi và sự xuất hiện của vi khuẩn kháng thuốc.
Họ áp dụng nguyên tắc "bác sĩ thú y chỉ sử dụng kháng sinh khi cần thiết" và nghiêm cấm sử dụng kháng sinh làm chất kích thích tăng trưởng. Chính phủ Đan Mạch đã ban hành các quy định nghiêm ngặt về kê đơn kháng sinh, yêu cầu bác sĩ thú y phải khám lâm sàng trước khi kê đơn. Họ cũng thiết lập hệ thống "thẻ vàng" (Yellow Card) để theo dõi việc sử dụng kháng sinh ở từng trang trại, từ đó đưa ra cảnh báo và hướng dẫn cụ thể khi phát hiện dấu hiệu lạm dụng.
Một nghiên cứu năm 2017 trên tạp chí Preventive Veterinary Medicine trên 202 trang trại lợn Đan Mạch đã chỉ ra các biện pháp giảm kháng sinh phổ biến nhất sau khi "thẻ vàng" ra đời là tăng cường vắc xin, đồng thời giảm trực tiếp việc sử dụng kháng sinh ở cả nhóm bác sĩ và nông dân. Kết quả là lượng kháng sinh đường uống giảm 89%, góp phần vào sự giảm trong tổng lượng kháng sinh sử dụng. Nghiên cứu cũng cho thấy không có xu hướng chọn các sản phẩm kháng sinh có liều lượng cao hơn để lách luật.
Nhờ những nỗ lực này, Đan Mạch đã giảm đáng kể lượng kháng sinh sử dụng trong chăn nuôi. Từ năm 1992 đến năm 2008, việc sử dụng kháng sinh trên mỗi kilogram lợn nuôi đã giảm hơn 50%, trong khi năng suất chung tăng lên. Kết quả này cho thấy chính sách kiểm soát kháng sinh của Đan Mạch không chỉ giúp giảm lượng kháng sinh sử dụng, hạn chế sự lan rộng của vi khuẩn kháng thuốc, bảo vệ sức khỏe cộng đồng mà còn chứng minh được việc sử dụng kháng sinh để tăng trọng vật nuôi là không cần thiết.
8. Kết lại
Cuộc chiến giữa nhân loại và các "siêu khuẩn" kháng kháng sinh không chỉ là một bài kiểm tra về khả năng y học, mà còn là thử thách về trách nhiệm và sự đoàn kết toàn cầu. Với những công cụ hiện có như các kháng sinh mạnh mẽ, công nghệ sinh học tiên tiến, vaccine hiệu quả và các chính sách quản lý bền vững, con người vẫn còn cơ hội giành lợi thế trong trận chiến này.
Nhưng Trang tin rằng, chỉ như vậy thôi thì chưa đủ. Vì siêu khuẩn không ngừng "học hỏi" và biến hóa, chúng ta cũng cần phải linh hoạt, sáng tạo và nhanh nhạy hơn trong từng "nước đi" của mình.
Trang luôn nghĩ, đây không chỉ là câu chuyện của các nhà khoa học trong phòng thí nghiệm hay các bác sĩ nơi bệnh viện. Đây là câu chuyện của tất cả chúng ta - những người mỗi ngày góp phần vào bức tranh kháng kháng sinh, dù là qua việc dùng thuốc, mua thực phẩm, hay chỉ là chăm sóc sức khỏe cho bản thân. Từng hành động nhỏ, như dùng kháng sinh đúng liều, hay thậm chí là hạn chế lãng phí thức ăn, cũng có thể trở thành một bước tiến nhỏ để đẩy lùi "siêu khuẩn."
Còn trong trị mụn nếu chưa thực sự cần thì đừng đụng vào kháng sinh mà có thể cân nhắc các hoạt chất phi kháng sinh an toàn hơn như nano bạc, terpinen-4-ol chẳng hạn, kết hợp phòng bệnh hơn chữa bệnh (bớt thức khuya, bớt buồn bực, siêng giặt vỏ áo gối,…bla…)
Rồi, tạm hết bài. Hẹn ae bài sau Trang sẽ bàn thêm về tình trạng mụn kháng kháng sinh - một nguyên nhân có thể gây nên tình trạng mụn mãi không hết.
__________________________
Thông tin liên hệ
Fanpage: https://www.facebook.com/latrang.co
Tiktok: https://www.tiktok.com/@latrang.co
Instagram: https://www.instagram.com/latrang.co/
Twins Skin Vietnam: https://www.facebook.com/twinsskin.vn
Trong Vietnam: https://www.facebook.com/profile.php?id=61568318274438
__________________________
Bài viết được thực hiện bởi Là Trang và team cộng sự. Thuộc quyền sở hữu của Là Trang và group Đồng Điệu (Sống đơn thuần - Đẹp đơn giản). Đề nghị không sao chép dưới mọi hình thức khi chưa có sự đồng ý của tác giả.

![[Phần 1] Mụn kháng kháng sinh: Tổng quan - Cuộc chiến kháng kháng sinh: Truyện sử của những “siêu khuẩn”](/content/images/2025/04/Cover-web---ng--i-u-logo-06.png)













Discussion